前言
脉冲电场消融因其更好的安全性和不劣于传统消融的有效性,正在迅速成为心律失常消融领域的新选择,据有源医疗设备展Medtec调查发现,短短几年时间,欧洲已积累了超过7万例的Farapulse真实世界案例。近日,Europace新近发表的一篇综述总结了PFA的机制和临床应用进展,强调了其相较于传统消融的潜在优势。

概述
脉冲场消融(PFA)是心脏电生理学领域治疗心律失常的一种创新方法。与射频或冷冻能量产生损伤的基质不同,PFA利用脉冲电场诱导细胞产生不可逆的电穿孔,导致靶组织破坏。这篇最新的综述总结了PFA的生物物理学原理和临床应用,突出了其相对于传统消融方法的潜在优势。讨论了当代PFA器械的临床数据,较好的临床结果和较低的临近损伤。总体而言,这些技术发展推动了当代PFA导管的快速发展。
一、电穿孔原理
当细胞暴露在足够强的电场下时,通过向组织输送高电压电脉冲,会在细胞膜上产生跨膜电压,导致孔的形成、脂质氧化和蛋白质损伤,使细胞膜的通透性增加,包括钠离子和钾离子在内的离子和分子会流入和流出细胞,包括钙离子内流(脑补下心肌细胞除极时的内外离子流动)。与此同时,已知会触发组织免疫反应的DAMP分子会从细胞中泄漏出来。钙离子的流入会触发其他次级过程,如细胞骨架的收缩和解体,并导致ATP耗尽。在膜重新密封后,其导电性仍然比电穿孔前略大。细胞通过触发其修复机制来恢复其稳态,包括热休克蛋白在内的修复机制。细胞死亡取决于电穿孔的强度,可能在暴露于电脉冲后迅速或立即发生,也可能在几小时甚至几天后发生。上述过程可以持续数纳秒至数百微秒,并可持续数小时。
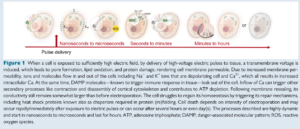
电穿孔引起的细胞死亡最常归因于三磷酸腺苷(ATP)耗竭、蛋白质损伤,例如离子通道和钙超载,更普遍地归因于细胞稳态的丧失。通过电穿孔进行的心脏消融通常被描述为非热和心脏组织选择性,但也应更客观的看待这些问题,也就是说,如果高压脉冲通过血池中的导管(1500-3000 V)传递到组织,将从发生器中汲取相当大的电流(10-20 A)——一些加热是不可避免的。它将与局部电场和电流密度的乘积成正比,就像射频消融一样:非热性质来自于细胞被电穿孔而不是加热致死的事实,因为电穿孔仅需要微秒甚至更短的时间,在如此短的时间内,无法显着加热组织。然而,如果连续传递多组重复脉冲,则可能会导致局部温度显着升高,并且 PFA 的“非热”特性将消失。值得注意的是,可能位于高电场中的细胞(例如红细胞)也有可能会被电穿孔损伤。
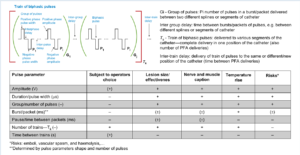
大多数脉冲参数是由制造商在系统(脉冲发生器和导管)的开发、测试和优化过程中选择的,并且因 PFA 系统不同而有所差异。这些脉冲参数(电压、脉宽、脉冲数量、间期和脉冲间延迟时间等)可能对有效性和安全性产生深远影响:病变大小、电极/导管击穿风险、气泡形成、温升和潜在热损伤、电弧 、气压伤风险和栓塞风险,因此术者通常无法更改,这些参数往往是锁定的。在大多数系统中,操作员几乎没有选择,而且这些选择的范围有限,并且有一些限制。在PFA过程中,只剩下很少的参数可以控制,比如:脉冲的次数、两次放电之间的时间(通常优选较长的时间,以避免由于堆积效应而导致温度升高)和电压(脉冲幅度)等。然而,必须强调的是,影响和风险通常与脉冲参数呈非线性关系,并且许多结果(影响和风险)取决于多个参数。波形和脉冲参数的优化可以被认为是存在相互冲突的多参数优化。
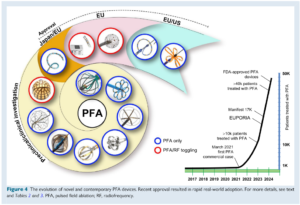
许多的PFA导管、设计和发生器正在开发中,并处于各阶段的临床研究中(表2和3以及图4)。由于临床需要,迄今为止大多数导管都被设计用于治疗房性心律失常,但心室消融将在不久的将来成为焦点。简而言之,当代导管可分为(i)环肺静脉隔离工具或(ii)逐点消融器械。在逐点消融器械中,可以使用新颖的具有较大消融范围的专用导管或传统的射频导管,使用PFA作为替代能源。由于该领域的快速发展,无法讨论所有PFA器械,但显示了不同类别的导管和发展阶段(图4)
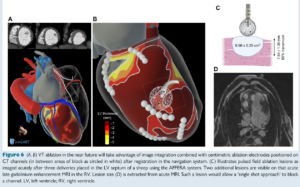
PFA导管与现有三维标测系统的集成有望在不久的将来成为现实。它可以提供更精确的PFA,从而减少gap风险。到目前为止,只有AFFERA™和最近的Varipulse™提供了三维标测功能。Farapulse ™导管与特定三维标测系统的集成正在开发中,预计不久将上市(图5D)。特定软件可提供关于接触、导管显示和消融范围、透壁性和持久性等的信息。
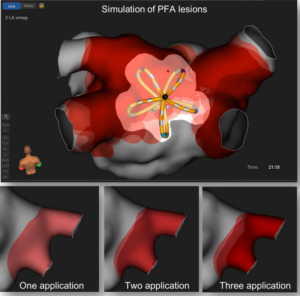 肺静脉隔离可能是绝大多数阵发性房颤患者唯一需要的策略。初步临床PFA经验表明,持续肺静脉隔离率较高,术者依赖性较低。这可能有助于提高未来的可预测的消融成功率。然而,持续性房颤的消融策略远不成熟,除肺静脉隔离外,尚无共识。目前尚不清楚一种策略是否适用于所有临床情况。脉冲场消融可能有助于了解房颤复发是由于标测还是消融不足所致。重要的是,PFA易于操作且功能强大,因此最佳消融策略是消融更少的区域以恢复窦性心律,PFA目前在后壁、二峡、三峡等领域表现良好,且持久性较好。
PFA提供了更安全、更快速、可能更持久的损伤,在未来可能为探索房颤消融的主要问题提供了机会:
(1)房颤消融中肺静脉隔离后转窦vs.肺静脉隔离无应答者·
阵发性和持续性房颤中肺静脉隔离后转窦的真实的比率是多少?
线性病变:需要更多的安全性和有效性数据,尤其是二尖瓣峡部(例如,CS内的局灶性PFA)
(1)减少组织损伤:通过高压电脉冲靶向特定心脏细胞,PFA技术能够减少对周围健康组织的损害。
(2)更短的手术时间:PFA手术时间较短,这使得医生能够处理更多病例,提高医院的资源利用率。
(3)潜在更高的安全性:临床研究表明,PFA在安全性方面可能优于RFA和冷冻消融,降低了并发症的风险。
在心房消融时,一些非典型折返或局灶性靶点包括小梁化区域,因为复杂的解剖,通常难以使用射频进行消融,脉冲场消融的优势是治疗类似的pouch和脊,它提供了理论上的优势,但这必须在临床实践中得到证实。如果需要在膈神经附近进行消融,PFA可能成为首选的能量来源。使用PFA治疗三尖瓣环峡部裂是有效的,尽管有记录在案的不良事件,如冠状动脉痉挛。值得注意的是,冠状动脉内/静脉硝基甘油的主动给药已被证明可显著减轻血管痉挛。
尽管PFA已在AF患者中进行了随机试验,但关于PFA心室消融的数据仍然很少,特别是在梗死心肌中。剂量仍不清楚,必须针对不同器械和解剖位置进行研究。AFFERA™导管,可产生深达12 mm的损伤,这对间隔或中间/心外膜消融至关重要,尤其是较厚的区域时。另一方面,证明PFA在瘢痕组织中的疗效将是关键,以及可能合适的能量(图6)。靶靶点位置(包括组织厚度以及纤维化和脂肪的存在)可能会影响PFA发放的的剂量/次数。重复使用PFA是增加当前系统损伤深度和宽度的唯一方法。
肺静脉隔离可能是绝大多数阵发性房颤患者唯一需要的策略。初步临床PFA经验表明,持续肺静脉隔离率较高,术者依赖性较低。这可能有助于提高未来的可预测的消融成功率。然而,持续性房颤的消融策略远不成熟,除肺静脉隔离外,尚无共识。目前尚不清楚一种策略是否适用于所有临床情况。脉冲场消融可能有助于了解房颤复发是由于标测还是消融不足所致。重要的是,PFA易于操作且功能强大,因此最佳消融策略是消融更少的区域以恢复窦性心律,PFA目前在后壁、二峡、三峡等领域表现良好,且持久性较好。
PFA提供了更安全、更快速、可能更持久的损伤,在未来可能为探索房颤消融的主要问题提供了机会:
(1)房颤消融中肺静脉隔离后转窦vs.肺静脉隔离无应答者·
阵发性和持续性房颤中肺静脉隔离后转窦的真实的比率是多少?
线性病变:需要更多的安全性和有效性数据,尤其是二尖瓣峡部(例如,CS内的局灶性PFA)
(1)减少组织损伤:通过高压电脉冲靶向特定心脏细胞,PFA技术能够减少对周围健康组织的损害。
(2)更短的手术时间:PFA手术时间较短,这使得医生能够处理更多病例,提高医院的资源利用率。
(3)潜在更高的安全性:临床研究表明,PFA在安全性方面可能优于RFA和冷冻消融,降低了并发症的风险。
在心房消融时,一些非典型折返或局灶性靶点包括小梁化区域,因为复杂的解剖,通常难以使用射频进行消融,脉冲场消融的优势是治疗类似的pouch和脊,它提供了理论上的优势,但这必须在临床实践中得到证实。如果需要在膈神经附近进行消融,PFA可能成为首选的能量来源。使用PFA治疗三尖瓣环峡部裂是有效的,尽管有记录在案的不良事件,如冠状动脉痉挛。值得注意的是,冠状动脉内/静脉硝基甘油的主动给药已被证明可显著减轻血管痉挛。
尽管PFA已在AF患者中进行了随机试验,但关于PFA心室消融的数据仍然很少,特别是在梗死心肌中。剂量仍不清楚,必须针对不同器械和解剖位置进行研究。AFFERA™导管,可产生深达12 mm的损伤,这对间隔或中间/心外膜消融至关重要,尤其是较厚的区域时。另一方面,证明PFA在瘢痕组织中的疗效将是关键,以及可能合适的能量(图6)。靶靶点位置(包括组织厚度以及纤维化和脂肪的存在)可能会影响PFA发放的的剂量/次数。重复使用PFA是增加当前系统损伤深度和宽度的唯一方法。
 有源医疗设备展Medtec认为,脉冲场消融代表了心脏电生理学领域的一种潜在的颠覆性技术,越来越多的证据支持其有效性和安全性,PFA的定位可能不仅仅是一种传统热消融的替代方案。然而,还需要更多的研究和临床经验的积累。
有源医疗设备展Medtec认为,脉冲场消融代表了心脏电生理学领域的一种潜在的颠覆性技术,越来越多的证据支持其有效性和安全性,PFA的定位可能不仅仅是一种传统热消融的替代方案。然而,还需要更多的研究和临床经验的积累。